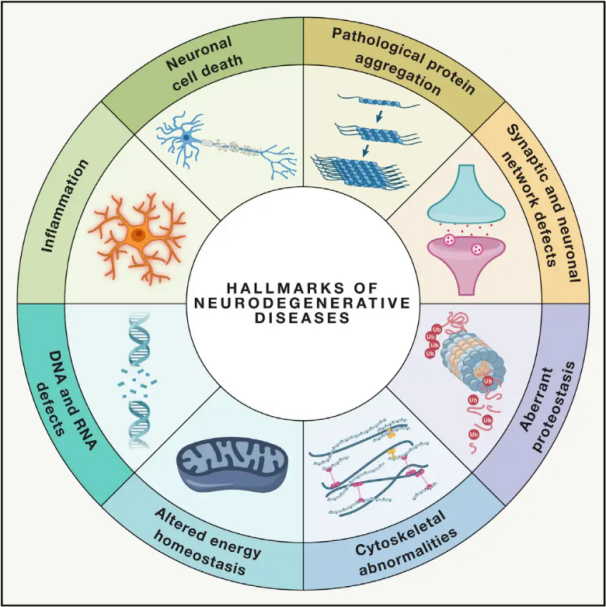
Neŭrodegeneraj malsanoj(NDM) karakteriziĝas per la progresema aŭ persista perdo de specifaj vundeblaj neŭronaj populacioj ene de la cerbo aŭ mjelo. La klasifiko de NDM povas baziĝi sur diversaj kriterioj, inkluzive de la anatomia distribuo de neŭrodegenero (kiel ekstrapiramidalaj malsanoj, frontotempa degenero aŭ spinocerebelaj ataksioj), primaraj molekulaj anomalioj (kiel amiloido-β, prionoj, taŭo aŭ α-sinukleino), aŭ gravaj klinikaj trajtoj (kiel Parkinson-malsano, amiotrofa lateralsklerozo kaj demenco). Malgraŭ ĉi tiuj diferencoj en klasifiko kaj simptomprezento, malsanoj kiel Parkinson-malsano (MP), Amiotrofa Lateralsklerozo (ALS) kaj Alzheimer-malsano (AM) dividas komunajn subestajn procezojn, kiuj kondukas al neŭrona misfunkcio kaj fina ĉelmorto.
Kun milionoj da homoj tutmonde trafitaj de NDD-oj, la Monda Organizaĵo pri Sano taksas, ke antaŭ 2040, ĉi tiuj malsanoj fariĝos la dua plej ofta kaŭzo de morto en industrilandoj. Kvankam ekzistas diversaj kuracadoj haveblaj por mildigi kaj administri la simptomojn asociitajn kun specifaj malsanoj, efikaj metodoj por malrapidigi aŭ kuraci la progreson de ĉi tiuj kondiĉoj restas neatingeblaj. Lastatempaj studoj indikas ŝanĝon en kuracaj paradigmoj de nura simptoma administrado al utiligado de ĉelaj protektaj mekanismoj por malhelpi plian plimalboniĝon. Ampleksa evidenteco sugestas, ke oksidativa streso kaj inflamo ludas ŝlosilajn rolojn en neŭrodegenerado, poziciigante ĉi tiujn mekanismojn kiel kritikajn celojn por ĉela protekto. En la lastaj jaroj, fundamenta kaj klinika esplorado malkaŝis la potencialon de Hiperbara Oksigena Terapio (HBOT) en la traktado de neŭrodegeneraj malsanoj.
Kompreni Hiperbaran Oksigenan Terapion (HBOT)
HBOT tipe implikas pliigi la premon super 1 absoluta atmosfero (ATA) — la premo je marnivelo — dum daŭro de 90-120 minutoj, ofte postulante plurajn kunsidojn depende de la specifa traktata kondiĉo. La plifortigita aerpremo plibonigas la liveradon de oksigeno al ĉeloj, kiu siavice stimulas la proliferadon de stamĉeloj kaj plibonigas la resaniĝajn procezojn mediaciitajn de certaj kreskofaktoroj.
Origine, la apliko de HBOT (Hiperbara Oksigena Terapeŭto) baziĝis sur la leĝo de Boyle-Marriott, kiu postulas la prem-dependan redukton de gasvezikoj, kune kun la avantaĝoj de altaj oksigenniveloj en histoj. Ekzistas gamo da patologioj konataj profiti de la hiperoksa stato produktita de HBOT, inkluzive de nekrozaj histoj, radiadaj vundoj, traŭmatoj, brulvundoj, kupeosindromo kaj gasgangreno, inter aliaj listigitaj de la Submara kaj Hiperbara Medicina Societo. Rimarkinde, HBOT ankaŭ montris efikecon kiel aldona kuracado en diversaj inflamaj aŭ infektaj malsanmodeloj, kiel ekzemple kolito kaj sepso. Konsiderante ĝiajn kontraŭinflamatoriajn kaj oksidativajn mekanismojn, HBOT ofertas signifan potencialon kiel terapia avenuo por neŭrodegeneraj malsanoj.
Antaŭklinikaj Studoj pri Hiperbara Oksigena Terapio en Neŭrodegeneraj Malsanoj: Komprenoj el la 3×Tg Musmodelo
Unu el la rimarkindaj studojfokusiĝis al la 3×Tg musmodelo de Alzheimer-malsano (AM), kiu montris la terapian potencialon de HBOT por plibonigo de kognaj deficitoj. La esplorado implikis 17-monat-aĝajn masklajn 3×Tg musojn kompare kun 14-monat-aĝaj masklaj C57BL/6 musoj servantaj kiel kontroloj. La studo montris, ke HBOT ne nur plibonigis kognan funkcion, sed ankaŭ signife reduktis inflamon, plakan ŝarĝon kaj Taŭ-fosforiligon — kritikan procezon asociitan kun AM-patologio.
La protektaj efikoj de HBOT estis atribuitaj al malpliiĝo de neŭroinflamo. Ĉi tio estis evidentigita per la redukto de mikroglia proliferado, astrogliozo, kaj la sekrecio de proinflamaj citokinoj. Ĉi tiuj trovoj emfazas la duoblan rolon de HBOT en plibonigado de kogna funkciado samtempe mildigante neŭroinflamajn procezojn asociitajn kun Alzheimer-malsano.
Alia antaŭklinika modelo uzis 1-metil-4-fenil-1,2,3,6-tetrahidropiridinajn (MPTP) musojn por taksi la protektajn mekanismojn de HBOT rilate al neŭrona funkcio kaj motoraj kapabloj. La rezultoj indikis, ke HBOT kontribuis al plifortigita motora agado kaj tenforto en ĉi tiuj musoj, korelaciante kun pliiĝo de mitokondria biogeneza signalado, specife per la aktivigo de SIRT-1, PGC-1α, kaj TFAM. Ĉi tio elstarigas la signifan rolon de mitokondria funkcio en la neŭroprotektaj efikoj de HBOT.
La Mekanismoj de HBOT en Neŭrodegeneraj Malsanoj
La subesta principo de utiligado de HBOT por NDD-oj kuŝas en la rilato inter reduktita oksigenprovizo kaj la malsaniĝemeco al neŭrodegeneraj ŝanĝoj. Hipoksio-induktebla faktoro-1 (HIF-1) ludas centran rolon kiel transkripcifaktoro, kiu ebligas ĉelan adaptiĝon al malalta oksigena tensio kaj estis implikita en diversaj NDD-oj, inkluzive de Alzheimer-malsano, Parkinson-malsano, Huntington-malsano kaj ALS, markante ĝin kiel decidan drogcelon.
Pro tio, ke aĝo estas signifa riskfaktoro por multoblaj neŭrodegeneraj malsanoj, esplori la efikon de HBOT sur maljuniĝa neŭrobiologio estas esenca. Studoj indikis, ke HBOT povas plibonigi aĝrilatajn kognajn deficitojn en sanaj pli maljunaj individuoj.Krome, maljunaj pacientoj kun signifaj memorkripliĝoj montris kognajn plibonigojn kaj pliigitan cerban sangofluon post eksponiĝo al HBOT.
1. Efiko de HBOT sur Inflamo kaj Oksidativa Streso
HBOT montris la kapablon mildigi neŭroinflamon en pacientoj kun severa cerba misfunkcio. Ĝi posedas la kapablon malsuprenreguligi proinflamatoriajn citokinojn (kiel IL-1β, IL-12, TNFα, kaj IFNγ) dum suprenreguligante kontraŭinflamatoriajn citokinojn (kiel IL-10). Kelkaj esploristoj proponas, ke reaktivaj oksigenaj specioj (ROS) generitaj de HBOT mediacias plurajn utilajn efikojn de la terapio. Sekve, krom ĝia prem-dependa vezik-redukta ago kaj la atingado de alta hista oksigena saturiĝo, la pozitivaj rezultoj ligitaj al HBOT parte dependas de la fiziologiaj roloj de la produktitaj ROS.
2. Efikoj de HBOT sur Apoptozo kaj Neŭroprotekto
Esplorado indikis, ke HBOT povas redukti hipokampan fosforiligon de p38 mitogen-aktivigita proteinkinazo (MAPK), poste plibonigante pensadon kaj malpliigante hipokampan difekton. Kaj memstara HBOT kaj en kombinaĵo kun Ginkgo biloba ekstrakto malaltigas la esprimon de Bax kaj la aktivecon de caspase-9/3, rezultante en malpliigitaj apoptozaj indicoj en ronĝulaj modeloj induktitaj de aβ25-35. Krome, alia studo montris, ke antaŭkondiĉado de HBOT induktis toleremon kontraŭ cerba iskemio, kun mekanismoj implikantaj pliigitan SIRT1-esprimon, kune kun pliigitaj niveloj de B-ĉela limfomo 2 (Bcl-2) kaj reduktita aktiva caspase-3, substrekante la neŭroprotektajn kaj kontraŭapoptotajn ecojn de HBOT.
3. Influo de HBOT sur la cirkulado kajNeŭrogenezo
Eksponado de subjektoj al HBOT estis asociita kun multoblaj efikoj sur la krania angia sistemo, inkluzive de plifortigo de la sango-cerba bariero-permeablo, antaŭenigo de angiogenezo kaj redukto de edemo. Aldone al pliigo de oksigenprovizoj al histoj, HBOTkreskigas vaskulan formadonper aktivigo de transkripcifaktoroj kiel vaskula endotela kreskofaktoro kaj per stimulado de la proliferado de neŭralaj stamĉeloj.
4. Epigenetikaj Efikoj de HBOT
Studoj rivelis, ke eksponiĝo de homaj mikrovaskulaj endotelaj ĉeloj (HMEC-1) al hiperbara oksigeno signife reguligas 8 101 genojn, inkluzive de kaj suprenreguligitaj kaj malsuprenreguligitaj esprimoj, elstarigante pliiĝon en genekspresio asociita kun antioksidaj respondaj vojoj.
Konkludo
La uzado de HBOT faris signifajn paŝojn laŭlonge de la tempo, pruvante ĝian haveblecon, fidindecon kaj sekurecon en klinika praktiko. Kvankam HBOT estis esplorita kiel ne-etikeda traktado por NDD-oj kaj iuj esploroj jam estis faritaj, restas urĝa bezono de rigoraj studoj por normigi HBOT-praktikojn en la traktado de ĉi tiuj kondiĉoj. Plia esplorado estas esenca por determini optimumajn traktadfrekvencojn kaj taksi la amplekson de utilaj efikoj por pacientoj.
Resumante, la intersekciĝo de hiperbara oksigeno kaj neŭrodegeneraj malsanoj montras promesplenan fronton en terapiaj eblecoj, pravigante daŭran esploradon kaj validigon en klinikaj kontekstoj.
Afiŝtempo: 16-a de majo 2025

